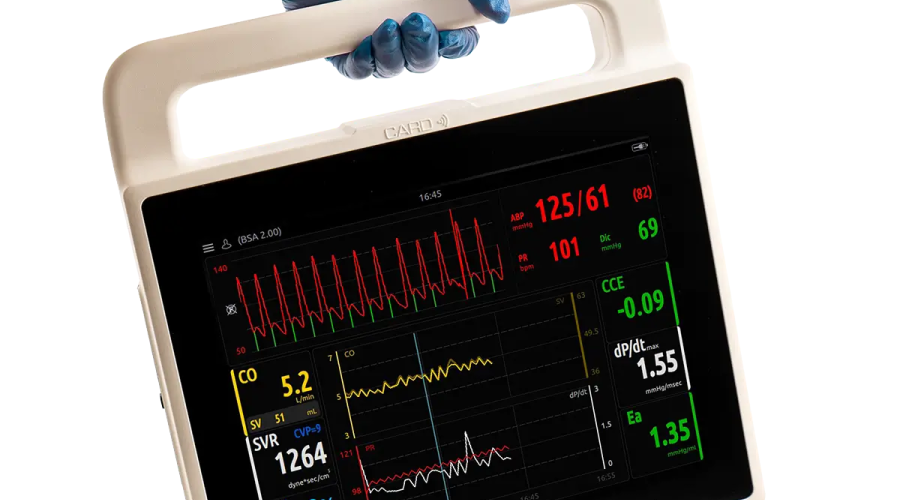
Porquê Débito Cardíaco?
Nas áreas de cuidados intensivos, onde os pacientes podem estar hemodinamicamente instáveis (ou em risco de instabilidade), os profissionais de saúde procuram otimizar a perfusão para evitar a disfunção de órgãos, a falência de vários órgãos ou mesmo a morte. Estas áreas referem-se a unidades de cuidados intensivos, áreas perioperatórias e outros locais onde podem ocorrer distúrbios circulatórios.
Nas áreas de cuidados intensivos, onde os pacientes podem estar hemodinamicamente instáveis (ou em risco de instabilidade), os profissionais de saúde procuram otimizar a perfusão para evitar a disfunção de órgãos, a falência de vários órgãos ou mesmo a morte. Estas áreas referem-se a unidades de cuidados intensivos, áreas perioperatórias e outros locais onde podem ocorrer distúrbios circulatórios.
Habitualmente, sempre que a perfusão se tornou importante, a pressão arterial (PA), especificamente a pressão arterial média (PAM), foi considerada como um substituto hemodinâmico fundamental para o fornecimento de oxigénio, sendo a hipotensão uma preocupação clínica, uma vez que está associada a uma deterioração dos resultados dos pacientes. No entanto, sabe-se agora que a hipotensão não conduz estritamente à hipoperfusão de órgãos e possui mecanismos fisiopatológicos subjacentes heterogéneos (Meng, 2021).
Se quebrarmos o conceito clínico de PA, existem dois determinantes: o débito cardíaco (DC) e a resistência vascular sistémica (RVS). A heterogeneidade subjacente à hipotensão relaciona-se com as potenciais alterações de ambos os determinantes da PA, pelo que a atuação terapêutica em cada cenário possível será diferente.
A literatura afirma cada vez mais que o DC não é apenas um determinante da PA, mas também se relaciona de forma forte e independente com a perfusão orgânica, enriquecendo a visão tradicional da perfusão resultante da pressão de perfusão dividida pelas resistências vasculares regionais. O DC é, em última análise, fornecido a vários tecidos e órgãos e a soma das suas quotas de perfusão corresponde ao DC (Meng, 2021).
O DC é determinado por necessidades metabólicas únicas e varia entre indivíduos. Assim, não existe uma referência de DC que se adapte a todos os pacientes. Embora a PA e o DC estejam fisiologicamente ligados, não há evidências de uma relação importante entre a pressão arterial e o DC em pacientes submetidos a procedimentos cirúrgicos, por exemplo. As evidências de gestão orientada do DC no perioperatório sugerem que a gestão orientada do DC pode reduzir as complicações e a mortalidade pós-operatórias, mas é necessário efetuar mais estudos, com maior robustez (Kouz et al., 2024).
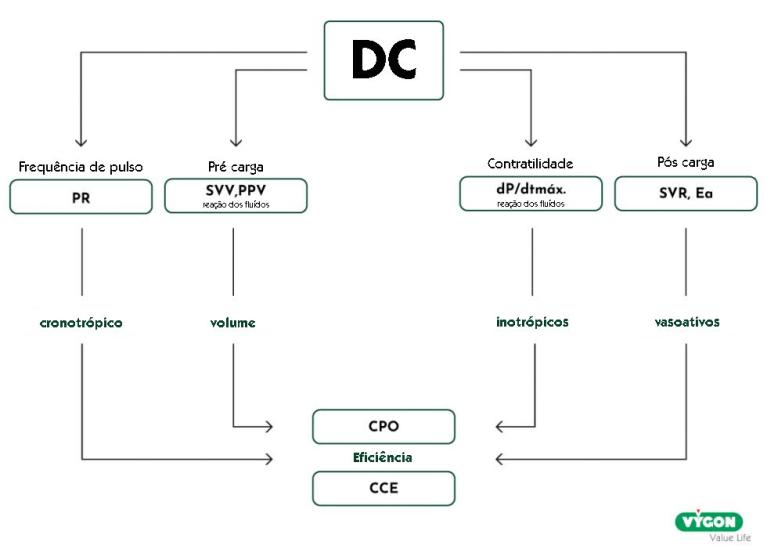
Através da monitorização do DC e dos seus determinantes (pré-carga, frequência cardíaca, pós-carga e contratilidade), é possível ter uma orientação e apoio adicional ao longo de diferentes etapas terapêuticas, como diagnósticos diferenciais (ex.: mecanismos de choque), tratamento e resposta, bem como avaliação contínua (Huygh et al, 2016). Através de valores hemodinâmicos mais avançados, pode-se simplesmente identificar as necessidades reais em curso do paciente, quer se trate de reanimação com fluído, vasopressores, agentes cronotrópicos ou inotrópicos, melhorando potencialmente os resultados do paciente ao agir de um modo mais proactivo e personalizado.
Existem vários métodos disponíveis para a monitorização do DC - incluindo a termodiluição da artéria pulmonar ou transpulmonar, a análise das ondas de pulso, o Doppler esofágico e as técnicas de biorreactância. A escolha da tecnologia dependerá sobretudo da sua aplicabilidade clínica, mas também dos conhecimentos e da abordagem do utilizador. Apesar da escolha do método de monitorização, continua a ser essencial uma compreensão fisiológica e fisiopatológica básica das variáveis hemodinâmicas relevantes (Kouz et al., 2024).
Como nota adicional, idealmente, a tecnologia de monitorização do DC deve ser fiável, contínua, não invasiva, independente do operador, rentável e ter uma resposta rápida. Os dispositivos de monitorização do DC devem ser progressivamente interligados com outros tipos de soluções de monitorização. A sustentabilidade ambiental associada a estes dispositivos é também cada vez mais considerada (de Waal et al., 2009; Kouz et al., 2024).
BIBLIOGRAFIA
- de Waal, Eric ECa et al. (2009). Cardiac output monitoring. Current Opinion in Anaesthesiology 22(1): p71-77. doi: 10.1097/ACO.0b013e32831f44d0
- Huygh, J. et al. (2016). Hemodynamic monitoring in the critically ill: an overview of current cardiac output monitoring methods [version 1; referees: 3 approved] F1000Research 5(F1000 Faculty Rev):2855. doi: 10.12688/f1000research.8991.1
- Kouz, K. et al. (2024). Haemodynamic monitoring during noncardiac surgery: past, present, and future. Journal of Clinical Monitoring and Computing (2024) 38:565–580. doi: 10.1007/s10877-024-01161-2.
- Meng, L. (2021). Heterogeneous impact of hypotension on organ perfusion and outcomes: a narrative review. British Journal of Anaesthesia, vol. 127, Issue 6, 845 – 86. doi: 10.1016/j.bja.2021.06.048
Autor: Joana Garcia
(Enfermeira Registada - Formadora Clínica e de Vendas @Vygon)